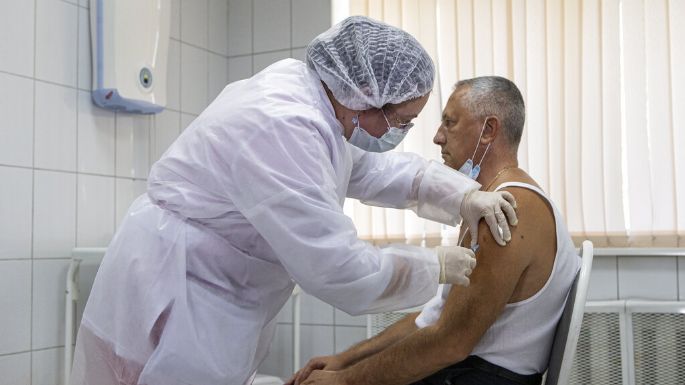
Rusia busca precalificación de la OMS para su vacuna Sputnik V
Autoridades rusas aseguran que esto permitirá que dicha dosis esté disponible para todo el mundo en un periodo de tiempo más corto.Rusia solicitó a la Organización Mundial de la Salud (OMS) acelerar el registro (“Emergency Use Listing”, EUL) y la precalificación de la vacuna Sputnik V, de acuerdo con información emitida hoy por el Fondo Ruso de Inversiones Directas (FIDR).
"Hemos presentado a la OMS una solicitud de registro acelerado y precalificación de la vacuna, lo que permitirá que Sputnik V se incluya en la lista de medicamentos que cumplen con los principales estándares de calidad, seguridad y eficacia", declaró Kirill Dmitriev, director del FIDR, en un comunicado.
Según el FIDR, el registro acelerado bajo el procedimiento EUL "permitirá que la vacuna rusa esté disponible para todo el mundo en un periodo de tiempo más corto en comparación con los procedimientos convencionales y respaldará los esfuerzos globales para prevenir la infección por coronavirus".
Con esta solicitud, Rusia se convierte en uno de los primeros países del mundo en pedir a la OMS este estatus para la vacuna contra el COVID-19.
A la vez, el Programa de Precalificación, organizado por la ONU y coordinado por la OMS, es el único programa mundial de garantía de la calidad de los medicamentos.
De modo que, en caso de recibir la precalificación, Sputnik V podría ser incluida en la lista de medicinas que utilizan organizaciones y países para gestionar su adquisición a gran escala.
Dmitriev recordó que Rusia fue el primer país del mundo en registrar una vacuna contra el COVID-19 y destacó que esta "se creó en base a una plataforma segura, eficaz y bien estudiada de vectores adenovirales humanos".
Sputnik V fue registrada el pasado 11 de agosto y actualmente se encuentra en la fase III de los ensayos, aunque ha sido recibida con recelo por la comunidad científica internacional debido a la rapidez de los ensayos y la poca información sobre el fármaco.
Con información de EFE.
sh