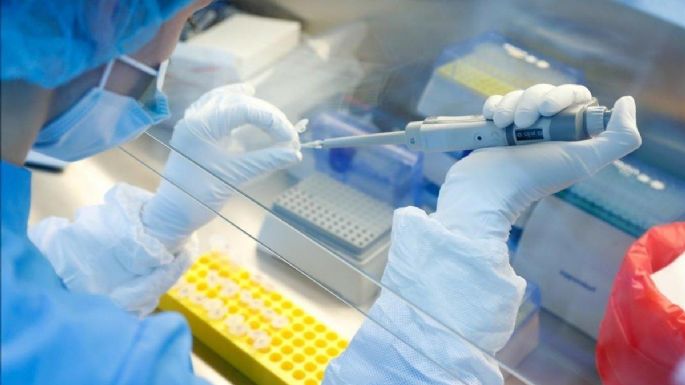
Pfizer solicita autorización de emergencia a la UE para vacuna contra COVID-19
El pasado 30 de noviembre, Moderna también solicitó la autorización de emergencia en Estados Unidos y Europa.Al igual que Moderna, Pfizer y su socio BioNTech solicitaron la autorización reglamentaria para su vacuna contra el nuevo coronavirus en la Unión Europea.
En este sentido, la Agencia Europea de Medicamentos (AEM) informó este martes que podría emitir una opinión antes de que finalice el año.
Detalló que se realizará una reunión –a más tardar el 29 de diciembre– sobre la evaluación programada.
Desde el pasado 6 de octubre comenzó un proceso de revisión continuo que permitió a la Agencia examinar los datos sobre la vacuna.
Con el objetivo de permitir que su regulador no necesite el permiso de su homólogo de la UE, el Reino Unido invocó una regla especial. Con ello, podría ser el primer país en aprobar el producto Pfizer-BioNTech.
Por su parte, Estados Unidos hará algo similar: el próximo 10 de diciembre habrá un panel de la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) donde se discutirá sobre la vacuna.
El pasado 30 de noviembre, Moderna también solicitó la autorización de emergencia en Estados Unidos y Europa.
Por Redacción Por Esto
EG